

现在大家提到益生元,总是关联益生菌,有益菌粮食的角色定位解释起来既容易也清晰,但今天有关益生元与免疫功能的相互关系的话题,我们暂且将两者剥离开来。

魏远安教授在首届微生态医疗创新论坛上
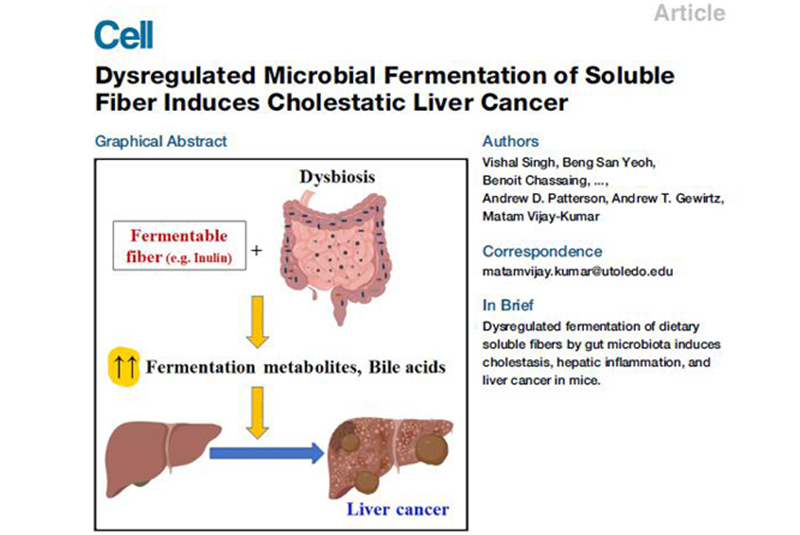
近期,《Cell》杂志文章《Dysregulated Microbial Fermentation of Soluble Fiber Induces Cholestatic Liver Cancer》的作者Kumar教授发表的一系列文章,提示我们不要忘记宿主细胞本身的作用,就如肠道上皮屏障,不只是单纯的物理性阻挡病原体入侵,而是有生命的、有选择性的。这种选择性就体现在免疫方面。
就好比一个人生病了,本质上不是人体内的细菌病了,而是人体内的细胞病了。又好比一个健康的战士在战场上中弹身亡,此刻,战士体内的肠道菌群依然存在,可战士的细胞已然死亡,如果我们说靠这些肠道菌群让这个战士起死回生,怕是要闹大笑话。所以,肠道菌群、宿主细胞与宿主免疫功能之间如何达到整体平衡?与益生元有什么关系?这就要在免疫方面找出原因。世上没有包治百病的神药,菌群也是一样的,要谈好坏,都需要有一定的边界条件。
首先要提到“免疫稳态”(Immunological Homeostasis)这个概念,免疫系统过强或者过弱都会对人的健康造成不好的影响,人体的免疫功能只有处在稳态才会健康。皮肤、肠道上皮等作为第一道屏障,受到病原体侵害后会向机体传递信息,召集免疫细胞过去对抗病原体。打个比方,两军交战,进攻一方发出信号,请求炮火支援,一阵炮火压制后,战士们开始冲锋,与另一方纠缠在一起并展开肉搏战,全歼对方后如果此刻再对阵地开炮,就会对己方造成伤亡。这就是自身免疫病对身体造成伤害的原因。免疫系统在人体全身都有分布,而与益生元关系较为密切的就是胃肠道方面的免疫稳态, Kumar教授在《Cell》杂志上发表了一系列的文章,所以他的观点并不是短期内形成的,而是不断演化而来的。文章的主要结论包括以下两点:
一、在菌群失调(T5KO小鼠)及其他极端的情况下(如长时间、大剂量、高脂饮食),可溶性膳食纤维助推有害菌的发酵, 可能诱发肝癌。
二、在菌群失调(T5KO小鼠)及其他极端的情况下(如长时间、大剂量、高脂饮食),菊粉等益生元改善肠道菌群失调的效果消失了。
关于肠道上皮屏障细胞TLRs信号通路的重要性,以前我们认为机体防御病原微生物侵染的天然免疫防线仅仅只是物理屏障,但是现在发现天然免疫对人体对抗病原体是十分重要的。天然免疫防线的第一步就是模式识别受体(Pattern Recognition Recpetors, PRRs)对病原体分子模式(Pathogen Associated Molecular Patterns, PAMPs)的识别。例如人的皮肤一旦划破,就需要由皮肤细胞向免疫细胞发送信号,免疫细胞才能到达现场。TLRs就是PRRs中的重要一员。TLRs接收到信息后,把信息转到到细胞核内,推动基因组转录细胞因子、炎症因子,再分泌到细胞外杀灭病原体,这就是我们看到的炎症、红肿。
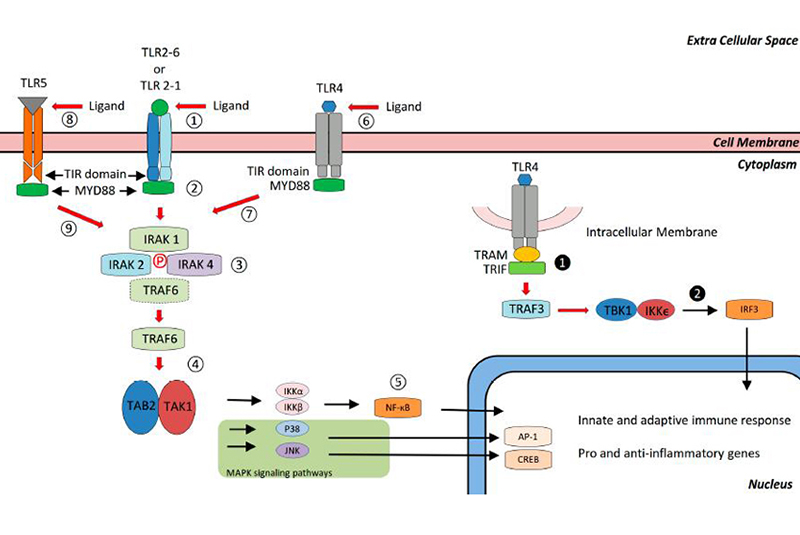
肠道上皮细胞TLRs信号通路与免疫应答
《Nature》2018年8月发表的一篇文章《Neonatal selection by Toll-like receptor 5 influences long-term gut microbiota composition》中提到:TLR5基因的敲除对小鼠肠道上皮屏障的天然免疫能力产生重大影响(特别是在生命的早期),宿主肠上皮细胞对肠道菌群的逆选择回路(counter-selective circuit)丧失,导致肠道菌群失衡,有害菌肠道定植增加。这一选择性会影响小鼠今后长期的肠道菌群构成。

TLR5的新生儿期选择性会影响长期的肠道菌群组成
该研究以未断奶的小鼠作为实验对象,相当于人类年龄的0-3岁。TLR5的一种确定的配体是鞭毛蛋白。TLR5敲除小鼠和野生型小鼠分别喂食带有鞭毛和不带鞭毛的沙门氏菌,结果发现对于TLR5敲除小鼠,有鞭毛的沙门氏菌大量定植在肠道;对于野生型小鼠,有鞭毛的沙门氏菌很少定植在肠道,差异十分明显。表明TLR5对肠道定植菌群有选择性。TLR、MyD 88和REG3ɣ 组成逆选择回路(counter-selective circuit),对早期婴儿肠道菌群定植有影响。这种影响是新生儿时期独有的,对肠道菌群重塑和人的一生有重要影响,这里推断可能是HMOs起到的重要作用。
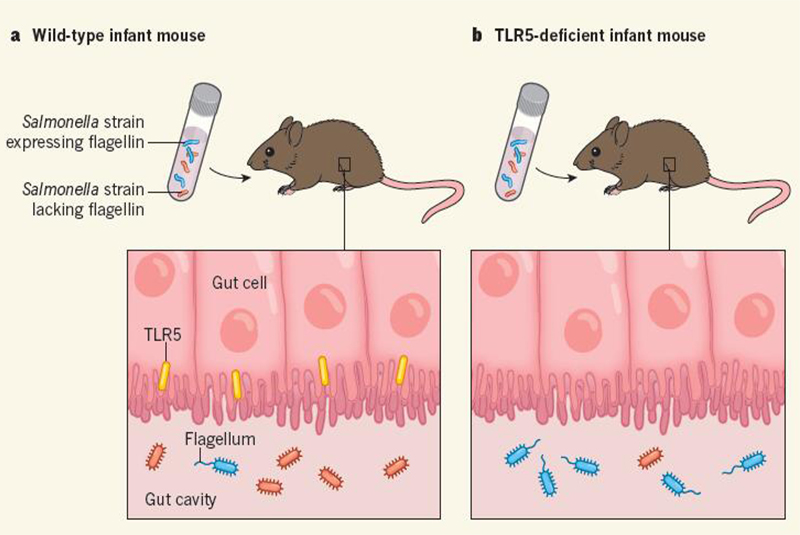
TLR5的选择性对肠道微生物组成的影响
另外一篇文章 《膳食益生元通过蛋白激酶 Cδ信号通路诱导强化肠道上皮细胞屏障功能》的结论是,两种已经商品化的益生元,菊粉和短链低聚果糖(scFOS),加入到肠道上皮细胞时,即使在益生菌不存在的情况下,也能直接促进屏障的完整性,阻止病原菌诱导的屏障毁坏。
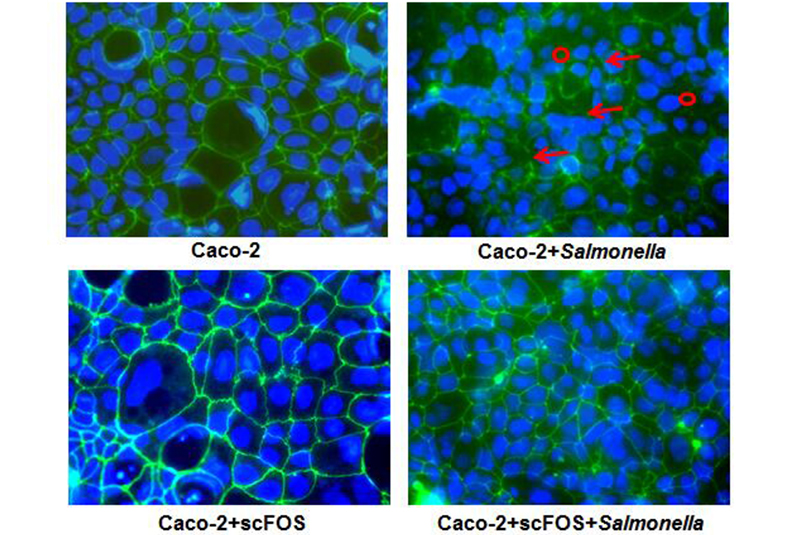
量子高科在低聚果糖益生元保护鼠伤寒沙门氏菌侵染下
肠道上皮细胞屏障方面的研究
这些效应与特定的紧密连接蛋白(TJ蛋白)的诱导有关,这种诱导作用是经TLRs信号途径启动, 并通过下游的蛋白激酶C(PKC)δ亚型相关的信号通路来进行的。在肠道上皮屏障TLRs信号途径受干扰或缺陷的情况下, 菊粉和低聚果糖直接促进肠道上皮细胞屏障的完整性,阻止病原菌诱导的屏障破坏的功能也将受损或消失。
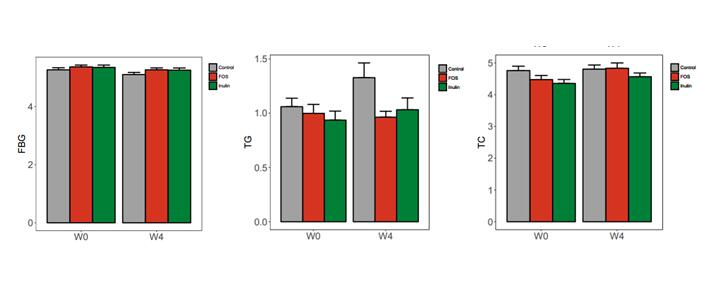
益生元(FOS)人群干预试验,量子高科与南方医科大学珠江医院合作项目
除了极端情况外,在普通情况的临床结果上,近年来,量子高科在与南方医科大学珠江医院合作的益生元(FOS)人群干预试验项目的结果表明,连续4周每天摄入15g 低聚果糖(FOS),不会引起空腹血糖、血脂的显著变化。另外,在益生元干预对疾病人群(2型糖尿病)肝功能影响的临床结果也表明,总胆红素TIL和谷丙转氨酶ALT均有转好趋势。再者,我们也认为丁酸盐悖论(butyrate paradox)值得进一步实验确证。
如果你能够认识到益生元在胃肠道免疫稳态上的响应机制和重要性,那么对《Dysregulated Microbial Fermentation of Soluble Fiber Induces Cholestatic Liver Cancer》(失调的微生物对可溶性纤维的发酵诱发胆汁淤积型肝癌)这篇文章,想必你就会有更深刻的认知。
一、在肠道上皮屏障TLRs信号途径受干扰或缺陷的情况下,宿主肠上皮细胞对肠道菌群的逆选择回路(counter-selective circuit)丧失,导致肠道菌群失衡,有害菌肠道定植增加。
二、在肠道上皮屏障TLRs信号途径受干扰或缺陷的情况下,菊粉和低聚果糖直接促进肠道上皮细胞屏障的完整性并阻止病原菌诱导的屏障毁坏的功能也将受损或消失。
除此之外,我们还要认识到,益生元调节菌群的作用是有大量科学根据的,小鼠与人体的代谢还是有差别的, 对动物实验结果的评估、解释和外推必须要科学和谨慎。正常情况下,可溶性膳食纤维的应用是安全的、有益的。
我们很欣慰的看到,Cell这篇文章中的实验方法和结果为益生元的精准化发展提供了范例和依据,值得借鉴。展望未来,精准、平衡、个性化和治未病将是益生元精准化发展方向上关键词。深入至分子细胞水平,明确益生元的作用机制,将有助于在免疫提升,定制个性化益生元配方和营养摄入方案,从而促进与保障人类健康。

--END--